Wir haben diesen Beitrag im laufenden Monat überprüft und die Beschreibungen teilweise aktualisiert.
Unsere Empfehlungen sind nach wie vor auf dem neuesten Stand. Letztes Updated am 10. April 2020
Die Folgen fehlender neutrophiler Leukozyten sind dramatisch. Ein Abfall der Neutrophilen unter 1000/μl führt zu einer erheblich gesteigerten Infektionsneigung. Wenn die Zahl der Neutrophilen (Stabund Segmentkernige) < 500/μl fällt, ist auch die Kontrolle der körpereigenen mikrobiellen Flora (z. B. in Mund und Darm) beeinträchtigt. Bei < 200/μl werden keine lokalen Entzündungsreaktionen mehr beobachtet. Eine Neutropenie entsteht durch die verminderte Bildung, den erhöhten Abbau oder ein exzessives peripheres Pooling dieser Zellen.
Eine abfallende Neutrophilenzahl oder ein signifikantes Absinken unter das Steady-state-Niveau sowie das Ausbleiben eines Anstiegs der Neutrophilenzahl im Rahmen von Infektionen oder anderen Stimuli erfordern eine eingehende Untersuchung des Patienten. Akute Neutropenien (z. B. durch Zytostatika) haben ein höheres Infektionsrisiko als über Monate oder Jahre anhaltende Neutropenien, die sich bei Infektionen oder durch eine streng kontrollierte Gabe von Endotoxinen bessern (siehe „Labordiagnostik und Management“).
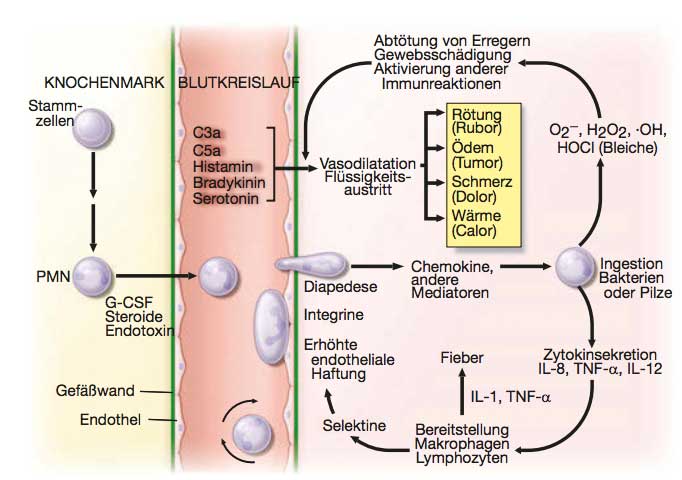
Schematische Darstellung der Entwicklung neutrophiler Granulozyten,
ihrer Rekrutierung und der Entzündungsreaktion. Die vier Hauptsymptome
der Entzündung (Rubor, Tumor, Calor und Dolor) sind ebenso dargestellt wie die Interaktionen
von Neutrophilen mit anderen Zellen und Zytokinen. G-CSF = Granulocyte Colony
Stimulating Factor; IL = Interleukin; PMN = segmentkernige Granulozyten; TNF-α =
Tumor-Nekrose-Faktor α.
Ursachen der Neutropenie
Einige Ursachen für angeborene oder erworbene Neutropenien sind in der Grafik oben aufgeführt. Am häufigsten treten Neutropenien iatrogen im Rahmen einer zytostatischen oder immunsuppressiven Therapie auf. Dabei werden vorübergehend die Stammzellen im Knochenmark geschädigt. Auch einige Antibiotika (Chloramphenicol, Trimethoprim-Sulfamethoxazol, 5-Flucytosin, Vidarabin) sowie die antiretrovirale Substanz Zidovudin können durch Inhibition der Proliferation von myeloischen Progenitorzellen eine Neutropenie verursachen. Azathioprin und 6-Mercaptopurin werden durch das Enzym Thiopurinmethyltransferase (TPMT) metabolisiert, dessen hypofunktioneller Polymorphismus, der bei 11 % der weißen Bevölkerung zu finden ist, zur Akkumulation von 6-Thioguanin und einer erheblichen Knochenmarktoxizität führen kann. Die Knochenmarkdepression hängt grundsätzlich von der Dosierung sowie der Dauer der Medikamentengabe ab. Nach Absetzen der auslösenden Substanz und Gabe von rekombinantem humanem G-CSF ist diese Form der Neutropenie meist reversibel.

Verminderte Bildung
- Arzneimittelinduziert – Alkylanzien (Stickstoff-Lost, Busulfan, Chlorambucil, Cyclophosphamid), Antimetaboliten (Methotrexat, 6-Mercaptopurin, 5-Flucytosin), nicht zytotoxische Substanzen (Antibiotika [Chloramphenicol, Penicilline, Sulfonamide], Phenothiazine, Tranquilizer [Meprobamat], Antiepileptika [Carbamazepin], Neuroleptika [Clozapin], bestimmte Diuretika, Thyreostatika, nicht steroidale Antiphlogistika)
- Hämatologische Erkrankungen – idiopathische und zyklische Neutropenie, ChédiakHigashi-Syndrom, aplastische Anämie, erbliche Gendefekte
- Knochenmarkkarzinose, Myelofibrose
- Mangelernährung – Vitamin-B12- und Folsäuremangel (insbesondere Alkoholiker)
- Infektionen (Tuberkulose, Typhus, Brucellose, Tularämie, Masern, infektiöse Mononukleose, Malaria, Virushepatitis, Leishmaniose, AIDS)
Gesteigerter peripherer Abbau
- Antineutrophile Antikörper und/oder „trapping“ in Lunge oder Milz
- Autoimmunerkrankungen – Felty-Syndrom, rheumatoide Arthritis, Lupus erythematodes
- Arzneimittel als Haptene – Aminopyrin, α-Methyldopa, Phenylbutazon, Quecksilberdiuretika, manche Phenothiazine
- Granulomatöse Polyangiitis
Transiente Neutropenie
- Schwere Sepsis (akute Endotoxinämie)
- Hämodialyse
- Kardiopulmonaler Bypass
Hereditäre Neutropenien
Hereditäre Neutropenien sind selten und können sich schon in der frühen Kindheit als ausgeprägte konstante Neutropenie oder auch als Agranulozytose manifestieren. Zu diesen Erkrankungen zählt das Kostmann-Syndrom (Neutrophile < 100/μl), welches meist fatal verläuft und durch eine Mutation im antiapoptotischen Gen HAX-1 verursacht wird. Die schwere chronische Neutropenie (Neutrophile 300– 1500/μl) wird durch eine Mutation der Neutrophilen-Elastase (ELA2) verursacht. Auch der hereditären zyklischen Neutropenie oder – genauer – der zyklischen Hämatopoese liegt eine Mutation der Neutrophilen-Elastase (ELA-2) zugrunde. Andere angeborene Neutropenien sind die Knorpel-Haar-Hypoplasie (Chondrodysplasia metaphysaria McKusick), welche durch eine Mutation der mitochondrialen RNS-prozessierenden Endoribonuklease RMRP ausgelöst wird, sowie das Shwachman-Diamond-Syndrom mit Pankreasinsuffizienz aufgrund einer Mutation im Shwachman-Bodian-Diamond-SyndromGen SBDS.
Auch das WHIM-Syndrom (Warzen, Hypogammaglobulinämie, Infektionen, Myelokathexis [= Retention von Leukozyten im Knochenmark]) gehört in diese Gruppe von Erkrankungen. Das WHIM-Syndrom ist durch eine Hypersegmentierung der Neutrophilen sowie eine Retention von myeloischen Zellen im Knochenmark gekennzeichnet und wird durch eine Mutation im Chemokin-Rezeptor CXCR4 verursacht. Auch andere Neutropenien mit Immundefekten wie die X-chromosomale Agammaglobulinämie, das Wiskott-Aldrich-Syndrom und der CD-40-Ligand-Mangel gehören in diese Gruppe. Mutationen im G-CSF-Rezeptor können auch zu einer schweren kongenitalen Neutropenie führen und sind mit der Entstehung von Leukämien assoziiert. Bei der retikulären Dysgenesie fehlen myeloide und lymphoide Zellen aufgrund von Mutationen des mitochondrialen Enzyms A
Neutropenie beim Neugeborenen
Die Neutropenie beim Neugeborenen kann mit mütterlichen Faktoren assoziiert sein. Die transplazentare Übertragung von IgG, welche gegen fetale Neutrophilenantigene gerichtet sind, kann zu peripherem Abbau führen. Auch die Einnahme von Medikamenten (z. B. Thiazide) während der Schwangerschaft kann durch verminderte Produktion oder verstärkten peripheren Abbau zu einer Neutropenie des Neugeborenen führen. Beim Felty-Syndrom (Trias aus rheumatoider Arthritis, Splenomegalie und Neutropenie) können in der Milz produzierte antineutrophile Antikörper die Lebensdauer der Neutrophilen verkürzen, während LGLs neutrophile Vorläuferzellen attackieren können. Eine Splenektomie kann beim Felty-Syndrom zu einem Anstieg der Neutrophilen und zu einem Abfall der antineutrophilen Antikörper führen. Bei einzelnen Patienten mit Felty-Syndrom ist die Neutropenie mit einer erhöhten Anzahl von LGL-Zellen assoziiert. Eine Splenomegalie mit peripherem Abbau von Neutrophilen wird auch bei lysosomalen Speicherkrankheiten und portaler Hypertension beobachtet.
Bildnachweis:
- Viktoriia Kasyanyuk 123rf.com
Ständig neue Beiträge
Wir bieten hier fachlich geprüfte Gesundheitsinformationen, die in allgemein verständlicher Sprache verfasst sind. Wir zeigen ausführliche Informationen zu Blutwerten, Laborwerten und beschreiben Krankheiten und deren Symptome, teils gibt es auch Therapiemöglichkeiten. Die textlichen und grafischen Inhalte dieses Portals werden ständig erweitert, sodass Sie hier und auf unserer Facebook Seite viele Gesundheitsinformationen finden.
• Unsere redaktionelle Qualitätssicherung • Beratung und Hilfe


